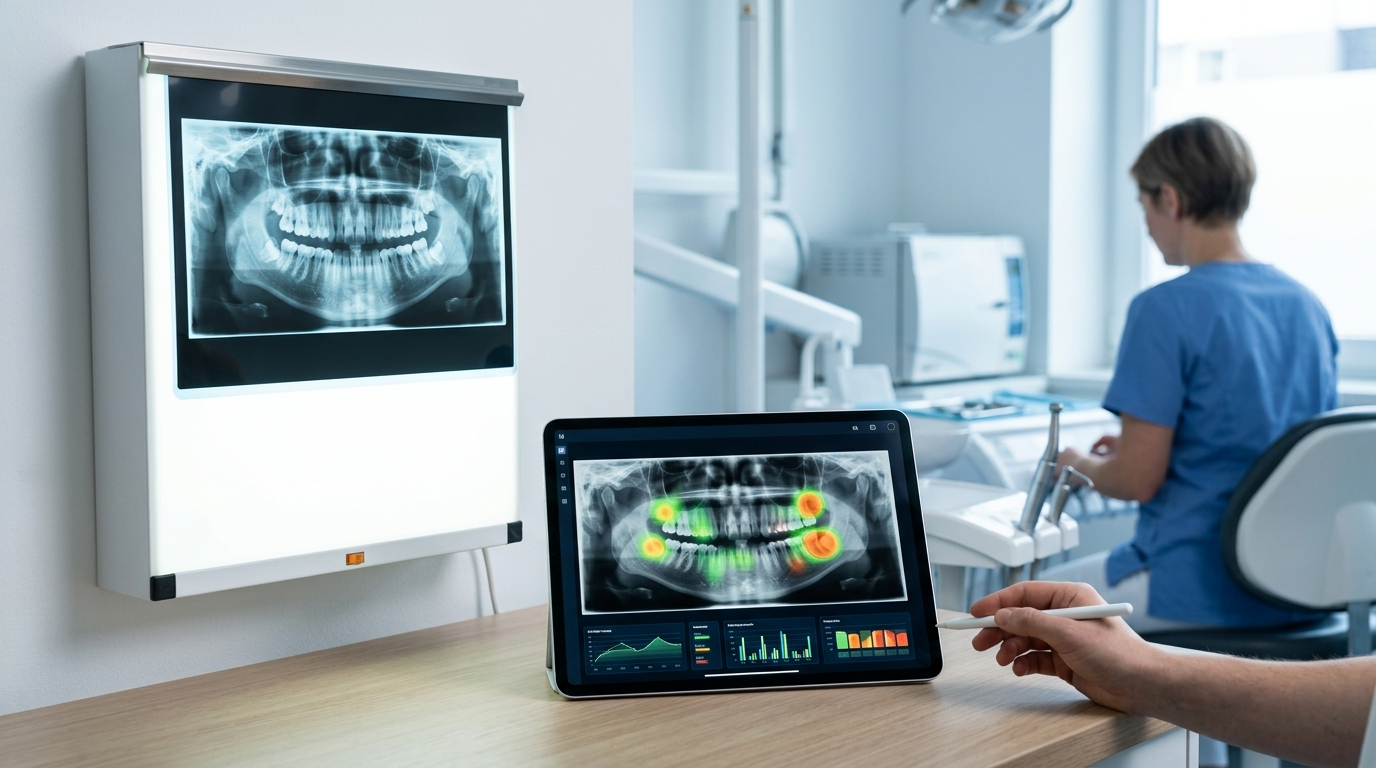
口腔がんAIスクリーニング——感度94%・特異度95%の実力と「盲点」を歯科医師が知るべき理由
歯科AIナビ編集部
2026年5月11日 · 📖 約7分
複数のメタ分析が感度94%・特異度95%という高い診断精度を報告し、AI口腔がんスクリーニングの技術的実現可能性は確立されつつある。しかし「見た目のないがん」を見落とすAIの盲点と、研究室と現場の精度ギャップは、歯科医師が今すぐ理解しておくべき臨床上の問題だ。
複数のメタ分析が示したコンセンサス——AIの口腔がん検出精度はどこまで来たか
2024〜2026年にかけて、査読済みのシステマティックレビューとメタ分析が集中して発表され、AI口腔がんスクリーニングの診断精度について明確なコンセンサスが形成されつつある。単発の研究成果ではなく、複数の独立したメタ分析が収束した数値として読むべきだ。
3本のメタ分析が描く精度の「帯域」
- ●センメルワイス大学チームによるJDR Clinical & Translational Research(2026年1月):最良のAIアーキテクチャで感度0.94(95%CI: 0.88–0.95)・特異度0.95(95%CI: 0.85–0.98)・DOR 212.391
- ●JISPCD(2025年9月):35研究・15,000件超の画像を解析したメタ分析でプール感度0.919(95%CI: 0.89–0.94)・特異度0.879(95%CI: 0.84–0.91)・AUC 0.9758・DOR 131.633
- ●Frontiers in Oral Health(2024年11月):18研究のメタ分析で感度0.87・特異度0.81・DOR 131.63・SROC-AUC 0.97582※ DOR 131.63・AUC 0.9758の値はソース2と3の両メタ分析に共通して報告されている
- ●3本の「帯域」の読み方:研究設計・画像モダリティ・対象疾患の違いにより感度は87〜94%の幅があるが、AUCは一貫して0.97超という水準で収束している
アーキテクチャ別では、CNN(畳み込みニューラルネットワーク)、特にEfficientNetB3が最上位の性能を示し、精度97.05%・感度96.92%・特異度97.17%を達成している8。Scientific Reports(2025年5月)に掲載されたDenseNet201モデルでは感度91.3%・AUC 0.97が報告されており4、複数のアーキテクチャで高水準の精度が確認されている。
「研究室」での数値が出やすい構造的理由
- ●病理組織像や統制された条件下で撮影した高品質臨床写真を使用すると感度・特異度が押し上げられやすい
- ●単一施設・同質データセットでの訓練と検証は、汎化性を過大評価するリスクをはらんでいる
- ●複数のメタ分析が共通して指摘する課題:「データの異質性と研究間の均一性欠如が汎化性・スケーラビリティ・再現性を制限している」
- ●現時点では検証的なランダム化比較試験(RCT)はなく、後方視的・横断的研究が主体である点にも留意が必要
なぜ「写真1枚」だけでは足りないのか——AIの2つの盲点
技術的ポテンシャルは明確だ。しかし「AIがあれば安心」という過信は、臨床上の危険な死角を生む。現在明らかになっているAIの盲点は2つある。
盲点① 撮影環境のばらつきで性能が激変する「現場品質問題」
- ●撮影者のスキルや撮影環境のばらつき——照明・アングル・フォーカスの不均一——がAIモデルの性能を大幅に低下させることは、複数の研究で繰り返し指摘されている
- ●未訓練者による撮影では、研究環境で示された高精度がそのまま再現されない。プレプリント段階の報告(medRxiv 2025年7月、未査読)では、制御された環境でのスマートフォン画像を用いたCNNモデルが精度94.29%・感度93.33%・AUC 0.99を示したが、著者自身が大規模臨床検証の必要性を認めている
- ●「研究室の精度 ≠ 自院の精度」:この原則を念頭に置き、照明・アングル・カメラ設定の標準化プロトコルを先に整備することが、将来のAI活用の前提条件になる
撮影品質の問題は、機器スペックではなく運用プロトコルの問題だ。AI製品が普及する前に、今の機材で「標準化された撮影」を習慣化することには意味がある。
盲点② 「見た目のないがん」はAIの死角——東京科学大学チームの警告
- ●東京科学大学(旧東京医科歯科大学)の研究チーム(心身歯科・口腔顎顔面外科腫瘍学などの部門)がBritish Dental Journal(2025年7月)に発表した論文10は、AIが持つ構造的な死角を明示した
- ●灼熱感・疼痛・異常感覚などの口腔灼熱症候群様の非特異的症状のみを呈し、視覚的病変を伴わない口腔扁平上皮癌(OSCC)は、AIが検出できない10
- ●「visual cues が absent(視覚的所見がない)な症例はAIが見落とす」——これは技術的な限界ではなく、画像認識というアプローチ固有の原理的な制約である
- ●患者が「なんとなく口の中が痛い・しびれる」と訴える場面は、受付での問診フォームや歯科衛生士との会話が最初の検出フィルターになる
写真を撮るだけでは届かない症例が存在する。問診・触診・視診の組み合わせがAIの前提条件であって、AIがその組み合わせを不要にするわけではない。
早期発見の意義を数字で確認する——「25.9%の壁」が意味すること
口腔がんは「見えるがん」だ。口腔内を直接視診できるという解剖学的優位があるにもかかわらず、診断の現実は驚くほど遅い。
局所段階で診断されているのは4人に1人だけ
- ●米国立がん研究所(NCI)のSEERデータベース(2025年)によると、口腔がん・咽頭がんのうち局所段階で診断されるのは25.9%のみ11
- ●局所段階での5年相対生存率:88.7%11
- ●遠隔転移後の5年生存率:約40%——局所段階との差は約49ポイントに上る
- ●「口腔内を毎回見ている歯科医師が最も早く気づけるはずなのに、4人中3人は局所段階を過ぎてから診断される」——この数字が、AIスクリーニングが解決しようとしているギャップの本質だ
日本の現状——「研究はあるが実装はまだ」
- ●2026年5月時点の本調査において、口腔がんスクリーニングを対象としたPMDA承認AI医療機器は確認されていない
- ●一方、東京科学大学チームがBDJに論文発表するレベルの研究力は国内に存在しており、基礎研究と臨床応用のギャップが課題として残る
- ●比較軸として:タイでは村落保健ボランティア(VHV)が運用するAIスマートフォンスクリーニングアプリ「RiskOCA」が地域実証済みであり(JMIR 2026年3月)9、低中所得国でのアクセス格差解消モデルとして機能している
- ●日本の歯科医師に今求められているのは「製品を待つ」姿勢ではなく「AIが機能するための土台を今から整える」準備だ
自院で今から始められる3つの準備——AIが来る前にやるべきこと
PMDA承認製品が現時点で存在しないことは、「何もしなくていい理由」にはならない。むしろ、製品が来たときに即座に活用できる院内体制を作るための時間が今ある。
今日からできること(所要15〜30分)
- ●【口腔粘膜の系統的観察プロトコルを文書化する(15分)】どの部位を・どの順序で・どの光源で確認するかを院内マニュアルに落とし込む。AI導入後の撮影標準化の下地になるだけでなく、現時点でも見落としリスクを下げる直接的な効果がある
- ●【既存の口腔内カメラで粘膜写真を撮影するフローを定例化する(初回30分)】新規患者の初診時に口腔粘膜を撮影・記録するルーティンを設定する。今すぐ臨床記録の質が上がり、将来のAI解析のための参照データにもなる
来月〜3ヶ月以内に準備すること
- ●【患者への「口腔粘膜検査」の告知を定期検診に組み込む】口腔がんへの社会的関心が高まっている今、定期検診に粘膜チェックを付加価値として明示することは、予防歯科としてのポジショニング強化にもつながる
- ●【受付・歯科衛生士へのブリーフィング(10分×1回)】AIが見落とす「症状のみの症例」に最初に気づけるのは、患者と会話するスタッフだ。「口の中がなんとなく痛い・しびれる」という訴えをどう拾うかを共有する
- ●【海外AI製品・国内研究動向のウォッチリストを設定する】Frontiers in Oral HealthとBritish Dental Journalのアラートを登録(無料)し、四半期ごとに5分でキャッチアップする習慣を作る。規制環境は今後急速に変わる可能性がある
この3つの準備に共通しているのは、AI製品の有無に関係なく「今すぐ臨床の質が上がる」という点だ。AIを待ちながら何もしないのではなく、AIを迎える側の体制を整えることが、今この時期の院長・歯科医師としての正しい動き方だ。
この記事のまとめ
AI口腔がんスクリーニングは複数のメタ分析で感度94%・特異度95%(JDR 2026年1月)に達したが、撮影品質依存の精度劣化と「視覚的病変を伴わないがん」という2つの盲点が臨床応用の課題として残る。局所段階での診断はいまだ25.9%(NCI SEER 2025)にとどまり、この壁を崩すためにも、日本の歯科医師が今すべきことは製品を待つことではなく、撮影標準化・問診強化・粘膜観察プロトコルの整備を通じてAIが機能する土台を自院に作ることだ。

口腔がんって「見えるがん」なのに、局所段階で見つかるのはまだ4人に1人だけ——そうなんですよね、この数字を見たとき、正直ぞっとしました。
私自身、定期検診での粘膜観察を「念のため」くらいの気持ちでやっていた時期があります。でも、AIの研究を追い始めてから、撮影して記録に残すことの意味が変わった気がしています。「AIが来たときのデータ」ではなく、「今日の見落としを防ぐ記録」として。
正解はないんですけど、まずは口腔内カメラで粘膜写真を1枚撮ることを定例化するだけでいい。製品が来てから動こうとすると、そのとき慌てることになりますよ。
AIを待ちながら、AIを迎える準備を。今週の初診で1枚撮ってみてください。
参考・出典
8件- [1]
Artificial Intelligence Helps Diagnose Oral Potentially Malignant Disorders: A Systematic Review and Meta-Analysis
https://pubmed.ncbi.nlm.nih.gov/41562124/参照: 2026-05-11 - [2]
Diagnostic performance of AI in detecting OPMDs and oral cancer: a systematic review and meta-analysis
https://www.frontiersin.org/journals/oral-health/articles/10.3389/froh.2024.1494867/full参照: 2026-05-11 - [3]
Diagnostic Accuracy of AI in Detecting OPMDs and Oral Cancer: A Meta-Analysis of Imaging-Based Studies
https://journals.lww.com/jpcd/fulltext/2025/09000/diagnostic_accuracy_of_artificial_intelligence_in.1.aspx参照: 2026-05-11 - [4]
Screening of OPMDs and oral cancer using deep learning models
https://www.nature.com/articles/s41598-025-02802-5参照: 2026-05-11 - [8]
Deep visual detection system for oral squamous cell carcinoma
https://www.nature.com/articles/s41598-025-34332-5参照: 2026-05-11
歯科医師・MBA / 株式会社HAMIGAKI 代表取締役
歯科医師としての臨床経験をベースに、AI×歯科経営の実践研究を行う。歯科AIナビを運営し、全国の歯科医師・院長へのAI活用支援に取り組む。